1. Vai trò của các xét nghiệm chẩn đoán trong đại dịch COVID-19
Giữa đại dịch COVID-19, nỗi sợ hãi đến từ chính sự mơ hồ, khi mà chúng ta không thể biết được rằng người đối diện có đang mang trong mình virus hay không, hay khi nào cuộc sống mới trở lại bình thường. Xét nghiệm, sàng lọc và giám sát chính là ba vũ khí của lực lượng tiền tuyến trong cuộc chiến chống lại đại dịch. Việc xét nghiệm giúp chúng ta sàng lọc được số ca nhiễm trong cộng đồng và nắm bắt kịp thời tình hình lây lan của virus tại khu vực, từ đó các cơ chế phòng dịch có thể được kích hoạt kịp thời để giám sát mức độ lây nhiễm và ảnh hưởng của đại dịch. Xét nghiệm hiệu quả còn giúp ngăn chặn sự bùng phát dịch bệnh trong cộng đồng thông qua chỉ định cách ly hoặc tự cách ly đối với những trường hợp tiếp xúc với các ca bệnh, hỗ trợ công tác truy vết quyết liệt và phát hiện những bệnh nhân không có hoặc chưa có triệu chứng nhưng vẫn có khả năng lây lan virus.
Bên cạnh đó, dữ liệu từ công tác xét nghiệm có thể xác định được tốc độ lây lan của virus SARS-CoV-2, thông qua việc tính hệ số R (thể hiện số lượng người trung bình bị lây nhiễm từ một người bị bệnh). Khi R lớn hơn 1, dịch bệnh sẽ lây lan theo cấp số mũ. Khi R nhỏ hơn 1 thì dịch bệnh đi vào giai đoạn thoái trào và cuối cùng là kết thúc. Dựa vào dữ liệu xét nghiệm và hệ số R, các nhà chức trách sẽ theo dõi sự lây nhiễm theo thời gian thực và tính toán thời điểm đỉnh dịch, từ đó xác định giai đoạn thực hiện hay nới lỏng các biện pháp phòng, chống lây lan dịch bệnh, cũng như thời gian và mức độ mở cửa lại nền kinh tế sao cho phù hợp với khả năng kiểm soát dịch bệnh của từng quốc gia [1].
2. Các phương pháp xét nghiệm chẩn đoán SARS-CoV-2 hiện tại
2.1. Xét nghiệm phân tử nhằm phát hiện virus
Loại phương pháp xét nghiệm phổ biến nhất hiện nay dựa trên phản ứng chuỗi polymerase (polymerase chain reaction - PCR), một loại xét nghiệm phân tử tìm kiếm các mảnh vật liệu di truyền của virus và xác định trường hợp đang nhiễm bệnh. Loại xét nghiệm này sử dụng các đoạn mồi đặc hiệu (primer) được tạo ra dựa trên dữ liệu gen của virus nhằm khuếch đại và phát hiện các đoạn thông tin di truyền đặc hiệu của virus SARS-CoV-2 như gene RdRP mã hóa cho các protein phi cấu trúc từ khung mở đọc ORF1a, gen protein vỏ (E), gen protein nucleocapsid (N) và gen protein gai (S) [2, 3]. Hầu hết các bộ kit xét nghiệm đều chứa hai hoặc ba thuốc thử, mỗi thuốc thử nhắm đến một đoạn gen riêng biệt. Do đó, chúng gần như miễn nhiễm đối với các thay đổi do đột biến trên trình tự gen của virus SARS-CoV-2, do khả năng đột biến xảy ra đồng thời trên tất cả các đoạn gen trên là rất nhỏ. Ngoài ra, các kỹ thuật xét nghiệm PCR tiên tiến hơn như xét nghiệm PCR sao chép ngược (RT-PCR) và xét nghiệm PCR thời gian thực (Real-time PCR), sử dụng tín hiệu huỳnh quang cho kết quả định lượng về tải lượng virus theo thời gian thực, cũng được ứng dụng trong xét nghiệm SARS-CoV-2 [4].
Các xét nghiệm PCR đối với SARS-CoV-2 hữu ích nhất trong giai đoạn đầu của bệnh vì chúng có thể phát hiện virus lên đến 2 ngày trước khi xuất hiện các triệu chứng [5]. RT-PCR có thể trả kết quả sau 3-4 giờ; tuy nhiên, quá trình này có xu hướng tốn nhiều thời gian hơn vì các mẫu phải được chuyển đến các phòng thí nghiệm an toàn cấp độ 3 do tính chất lây nhiễm của virus, khiến tổng thời gian quay vòng trung bình là từ 4-8 giờ.
2.2. Xét nghiệm huyết thanh nhằm phát hiện kháng thể
Dù chẩn đoán PCR được coi như tiêu chuẩn vàng cho xét nghiệm SARS-CoV-2 nhờ vào độ chính xác, một loại xét nghiệm chẩn đoán khác, có khả năng phân biệt giữa bệnh nhân đang nhiễm và người đã khỏi bệnh, cũng đang được sử dụng ngày càng rộng rãi hơn. Xét nghiệm huyết thanh hay còn gọi là xét nghiệm kháng thể là một xét nghiệm đánh giá phản ứng miễn dịch của cơ thể người mắc đối với virus bằng cách phát hiện kháng thể (immunoglobulin), bao gồm IgG và IgM, hoặc tổng lượng kháng thể trong mẫu máu, huyết tương, hoặc huyết thanh.
Xét nghiệm huyết thanh dựa vào cơ chế chìa khóa-ổ khóa đặc hiệu của kháng thể-kháng nguyên nhằm phát hiện kháng thể trong cơ thể bằng cách sử dụng kháng nguyên được thiết kế trong phòng thí nghiệm để bắt chước các cấu trúc virus, qua đó xác định được những người đã bị phơi nhiễm SARS-Cov-2 nhưng đã khỏi bệnh. Vì tính đặc hiệu của kháng nguyên với các kháng thể chống lại SARS-CoV-2 quyết định tính chính xác các xét nghiệm huyết thanh, các kháng nguyên này đã được áp dụng: protein gai (S), protein nucleocapsid (N) và vùng liên kết thụ thể nhắm vào enzym chuyển đổi angiotensin 2 (ACE2), là thụ thể cho cả SARS-CoV và SARS-CoV-2.
Các xét nghiệm huyết thanh SARS-CoV-2 trên thị trường bao gồm xét nghiệm định tính như xét nghiệm miễn dịch sắc ký nhanh [6] hoặc xét nghiệm định lượng kháng thể như xét nghiệm miễn dịch hấp thụ liên kết với enzym (ELISA) [7] và xét nghiệm miễn dịch phát quang hóa học (CLIA) [8], khác biệt ở cách chúng xác định nhận dạng kháng thể-kháng nguyên.
Thường mất một thời gian để cơ thể phản ứng với sự xâm nhập của kháng nguyên virus do đó có thể không xét nghiệm được kháng thể cho đến 6-7 ngày sau khi bắt đầu các triệu chứng. Vì vậy, khả năng áp dụng các xét nghiệm huyết thanh học được dùng cho các giai đoạn sau khi nhiễm bệnh. Tuy nhiên, khi quá trình bệnh kết thúc hẳn, tải lượng virus trong cơ thể không còn và xét nghiệm sẽ không còn hiệu quả. Do đó, các xét nghiệm kháng thể thường đạt được độ nhạy cao nhất sau 8 ngày từ khi nhiễm bệnh.
2.3. Phương pháp test nhanh tại chỗ (Point-of-care) cho xét nghiệm phân tử và huyết thanh
Với sự bùng phát nhanh chóng của COVID-19, sự trì hoãn gây ra bởi thời gian vận chuyển mẫu xét nghiệm đến các phòng thí nghiệm trở thành một rào cản lớn đối với việc mở rộng quy mô và tần suất xét nghiệm nhằm đáp ứng được nhu cầu cấp thiết trong công cuộc chống dịch. Do đó, phương pháp test nhanh tại chỗ (Point-of-care - POC) đã ra đời nhằm đem đến một giải pháp di động và nhanh chóng nhờ việc loại bỏ quá trình và thời gian gửi mẫu đến các phòng xét nghiệm tập trung và cho phép các khu vực không có cơ sở hạ tầng xét nghiệm như trung tâm y tế phường xã, khu cách ly hoặc ngay tại nhà người bệnh. Nhờ đó, thời gian chờ kết quả xét nghiệm có thể giảm từ hàng giờ hoặc thậm chí hàng ngày xuống chỉ còn vài phút, giúp đẩy nhanh quá trình sàng lọc, tăng tốc độ truy vết F0 và giảm tải khối lượng công việc đáng kể cho các trung tâm xét nghiệm.
Phương pháp POC đã được nghiên cứu và sản xuất cho cả hai loại xét nghiệm phân tử và huyết thanh. Các loại xét nghiệm POC phân tử giúp xác định các ca bệnh đang nhiễm có cơ chế tương tự phương pháp PCR nhưng được vận hành trong một hệ thống xử lý mẫu tự động khép kín, ví dụ như Abbott’s ID NOW, Cepheid’s Xpert Xpress, Bosch’s Vivalytic, kit Mesa Biotech’s Accula cầm tay, hoặc kit Cue Health’s dùng một lần (Hình 1) được khẳng định là sẽ cho kết quả trong vòng 5-45 phút. Những thiết bị này có thể đi kèm với các bộ kit để bệnh nhân có thể tự lấy mẫu tại nhà và gửi tới trung tâm y tế phường, xã để kiểm tra.

Ngoài ra, cũng có các loại xét nghiệm POC phân tử phát hiện trực tiếp kháng nguyên virus từ mẫu dịch mũi họng và dịch tỵ hầu. Phương án test kháng nguyên nhanh cộng với hình thức lấy mẫu gộp đã được Bộ trưởng Y tế Nguyễn Thanh Long quyết định sử dụng thay thế phương thức xét nghiệm RT-PCR truyền thống từ ngày 25/5/2021 với mục đích đưa F0 ra khỏi cộng đồng càng nhanh càng tốt. Hiện test nhanh kháng nguyên đang là dạng kit POC phổ biến nhất ở Việt Nam với vô vàn chủng loại được rao bán trên thị trường, tuy nhiên cho tới thời điểm hiện tại (7/2021) chỉ có 8 loại kit test nhanh nCoV được Bộ Y tế cấp phép (1 loại sản xuất trong nước, 7 loại nhập khẩu từ Hàn Quốc và Nhật Bản) [9].
Phương pháp POC cũng đã được dùng cho hình thức xét nghiệm huyết thanh và được thiết kế để sử dụng tại gia. Các thiết bị que thử nhanh ứng dụng kỹ thuật Lateral Flow Immunoassays dựa trên sắc ký đồ miễn dịch, tương tự như que thử thai. Các bộ dụng cụ xét nghiệm tại nhà này có thể phát hiện các kháng thể (IgM và IgG) từ mẫu máu lấy được bằng cách chích ngón tay và cho kết quả trong vòng chưa đầy 20 phút thông qua sự thay đổi màu sắc trên que thử (Hình 2) [10]. Nhiều sản phẩm đã được cấp phép sử dụng bởi FDA (Mỹ) như Cellex qSARS-CoV-2 IgG/IgM Rapid Test, Healgen COVID-19 IgG/IgM Rapid Test Cassette, Autobio Anti-SARS-CoV-2 Rapid Test or Chembio Diagnostic Systems DPP COVID-19 IgM/IgG System (Hình 3).
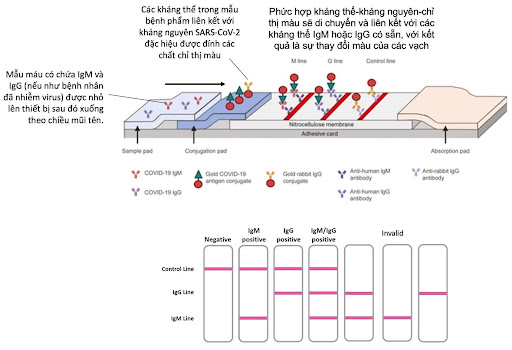
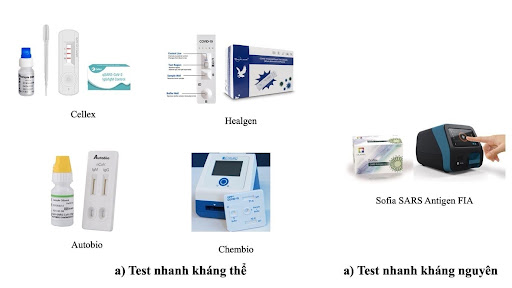
Tuy test nhanh kháng nguyên và các xét nghiệm tại nhà khác là những công cụ quan trọng đối với cuộc chiến chống dịch COVID-19 vì chúng có thể được thực hiện tại chỗ để giảm bớt áp lực về thông lượng xét nghiệm phân tử và đem lại hiệu quả về chi phí, cũng như sự tiện lợi, các xét nghiệm POC này vẫn thua kém các công cụ chẩn đoán truyền thống (xét nghiệm phân tử và xét nghiệm huyết thanh) về độ chính xác cũng như thiếu sự kiểm định chất lượng của Bộ Y tế trong việc sản xuất, nhập khẩu và lưu hành.
3. Thách thức đối với các phương pháp xét nghiệm SARS-CoV-2
3.1. Những yếu tố quyết định độ chính xác của các phương pháp xét nghiệm phân tử và xét nghiệm huyết thanh hiện nay
Sự thiếu chính xác trong các xét nghiệm chẩn đoán COVID-19 có thể xảy ra theo hai cách: kết quả âm tính giả xác định nhầm người mang bệnh là không nhiễm bệnh và kết quả dương tính giả chỉ định người khỏe mạnh thành bị nhiễm bệnh. Trong thực tế, sai sót trong kết quả xét nghiệm COVID-19 là không thể tránh khỏi, với từ 2% đến 29% trong tổng số xét nghiệm sẽ cho kết quả âm tính giả [12] và số lượng kết quả sai thậm chí sẽ còn lớn hơn khi quy mô thử nghiệm được mở rộng với hình thức dùng mẫu gộp và các kit test nhanh.
PCR hiện được coi là loại xét nghiệm chính xác nhất với độ nhạy khoảng 70-90% và độ đặc hiệu từ 95-100% [13]. Tuy nhiên, vẫn có nhiều nguyên nhân dẫn tới sự sai lệch trong kết quả PCR. Thứ nhất, lấy mẫu quệt bằng tăm bông có thể không thu thập đủ lượng virus để đạt ngưỡng phát hiện, đặc biệt ở giai đoạn đầu nhiễm bệnh và với những bệnh nhân không có triệu chứng. Người ta ước tính rằng trong vòng bốn ngày đầu tiên sau khi nhiễm bệnh khả năng nhận được kết quả âm tính cao hơn 67% [14]. Thứ hai, vị trí thu thập mẫu để xét nghiệm cũng là một yếu tố quyết định mức độ chính xác của kết quả. Phương pháp lấy mẫu phổ biến hiện nay là lấy mẫu ngoáy mũi và hầu họng, đờm hoặc dịch phế nang. Một số nghiên cứu đã khẳng định rằng lượng virus được tìm thấy chính xác nhất trong dịch phế quản-phế nang, tiếp theo là ở đờm, mũi và hầu họng với độ nhạy tương ứng là 93%, 72%, 63% và 32%. Một số nghiên cứu khác lại cho rằng các mẫu từ dịch tỵ hầu cho kết quả chính xác hơn so với mẫu đờm [15]. Nhưng do những hạn chế liên quan đến độ phức tạp của thao tác và phản ứng của bệnh nhân, phương pháp lấy mẫu phổ biến nhất trong bối cảnh hiện nay là lấy mẫu dịch tỵ hầu. Thứ ba, chất lượng của chính các que lấy mẫu cũng như điều kiện trữ mẫu, quản lý, phân phối và các quy trình lấy mẫu gộp không đúng cách cũng có thể dẫn đến kết quả bị lỗi và không nhất quán [16]. Thứ tư, do số lượng lớn các xét nghiệm PCR được tạo ra trong nháy mắt để đáp ứng nhu cầu thị trường, chất lượng thuốc thử có thể kém chất lượng, dẫn đến các sai sót trong kết quả xét nghiệm [17]. Nhìn chung, việc lấy mẫu bệnh thích hợp, tại đúng vị trí giải phẫu, đúng thời điểm ủ bệnh và sử dụng các xét nghiệm được kiểm định là rất quan trọng để quá trình xét nghiệm phân tử nhanh chóng và chính xác.
Xét nghiệm kháng thể cũng có một số vấn đề tương tự với xét nghiệm phân tử, chẳng hạn như việc xét nghiệm sớm có thể dẫn đến kết quả âm tính giả do nồng độ kháng thể chưa cao trong khi các xét nghiệm có độ nhạy cao như PCR cho kết quả dương tính. Một số xét nghiệm huyết thanh có độ đặc hiệu thấp, nghĩa là chúng cũng phản ứng với các kháng thể chống lại các bệnh nhiễm trùng khác, dẫn đến kết quả dương tính giả. Điều này có thể xuất phát từ phản ứng chéo của các kháng thể từ các coronavirus khác, vì người ta ước tính rằng 60-75% trẻ em đã mang kháng thể từ một hoặc nhiều coronavirus phổ biến khác, trong khi 90% người lớn trên 50 tuổi vẫn giữ được kháng thể đối với 4 chủng coronavirus đã từng xuất hiện [18]. Do đó, quan trọng là phải chọn đúng kháng nguyên thích hợp (khuyến nghị dùng protein gai S) để tăng tính đặc hiệu của các xét nghiệm huyết thanh học.
3.2. Việc kiểm định các thiết bị xét nghiệm
Không có xét nghiệm nào đưa ra kết quả chính xác 100%. Do đó, quy trình đánh giá và kiểm định bởi các cơ quan có thẩm quyền trước khi đưa thiết bị vào sử dụng là vô cùng cần thiết. Tuy nhiên, trong cuộc chạy đua giữa khoa học và virus, tốc độ thương mại hóa các xét nghiệm COVID-19 cũng như sự đa dạng của các sản phẩm cũng vô tình khiến cho các nỗ lực kiểm định trở nên khó khăn.
Tại thời điểm tháng 7/2021, Bộ Y tế đã cấp phép cho hơn 40 loại sinh phẩm cho các kỹ thuật xét nghiệm PCR, xét nghiệm kháng thể và test nhanh (theo Công văn 5288/BYT-TB-CT của Bộ Y tế). Trong đó, có 20 loại sinh phẩm cho xét nghiệm phân tử, 9 loại cho test kháng thể ELISA, 4 loại test nhanh kháng thể và 8 loại sinh phẩm cho test nhanh kháng nguyên (Bảng 1). Do đó, người dân cần chú ý chỉ mua những sản phẩm xét nghiệm đã được kiểm định để bảo đảm kết quả chính xác nhất.
Bảng 1. Thống kê các loại xét nghiệm đã được Bộ Y tế cấp phép tính đến tháng 7/2021
|
Sản xuất trong nước |
Nhập khẩu |
||
|
Xét nghiệm phân tử (kỹ thuật PCR hoặc LAMP) |
5 |
15 |
|
|
Xét nghiệm huyết thanh (kháng thể) |
2 |
7 |
|
|
Test nhanh |
Kháng thể |
2 |
2 |
|
Kháng nguyên |
1 |
7 |
|
3.3. Giá trị của “hộ chiếu miễn dịch” từ kết quả xét nghiệm kháng thể
Sau khi đại dịch COVID-19 đã tạm ngưng hoành hành tại một quốc gia, có hai vấn đề hiện đang được tranh luận: miễn dịch cộng đồng và việc sử dụng “hộ chiếu miễn dịch” cho các bệnh nhân COVID-19 đã khỏi bệnh. Cho tới nay, không có bằng chứng rõ ràng cho thấy con người có thể đạt được tình trạng miễn dịch với COVID-19 hoàn toàn và nếu việc đó có xảy ra thì việc khả năng ấy sẽ kéo dài trong bao lâu và hiệu quả bảo vệ của nó trước các biến chủng SARS-CoV-2 mới đang liên tục xuất hiện vẫn là câu hỏi bỏ ngỏ. Thực tế cho thấy một số dòng coronavirus như SARS có khả năng kích thích cơ thể sinh miễn dịch và duy trì bức màng bảo vệ này trong vài năm, khiến nhiều nhà khoa học tin rằng điều tương tự sẽ xảy ra đối với COVID-19. Dù vậy, WHO đã khuyến cáo rằng “hiện tại không có bằng chứng nào cho thấy những người đã mắc và khỏi COVID-19 cũng như đang mang trong người kháng thể sẽ được bảo vệ hoàn toàn trước nguy cơ tái nhiễm bệnh.” [19] và đã có một số trường hợp bệnh nhân được phát hiện dương tính với SARS-CoV-2 sau khi được cho là đã “hồi phục” [20]. Vì vậy, tình trạng miễn dịch tạm thời có thể sẽ không bảo vệ được người bệnh trước các biến chủng mới và tái nhiễm SARS-CoV-2. Do đó, trong lúc chưa có kết luận chắc chắn nào về tỷ lệ tái nhiễm, hoặc trước khi một loại vaccine hiệu quả ra đời, việc sàng lọc các cá nhân được coi là miễn dịch thông qua kháng thể và cấp các “hộ chiếu miễn dịch” này nói riêng và giá trị của xét nghiệm kháng thể nói chung vẫn mang ý nghĩa tương đối hạn chế về mặt an toàn sức khỏe đối với công cuộc chống lại đại dịch COVID-19.
3.4. Năng lực triển khai xét nghiệm
Kể từ khi WHO đưa ra yêu cầu tăng công suất xét nghiệm phân tử trong đại dịch COVID-19, việc các quốc gia ồ ạt tiến hành xét nghiệm diện rộng đã gây nên một làn sóng lo ngại về năng lực xét nghiệm của các nước có đáp ứng được các tiêu chuẩn chung nhằm từ đó đưa ra chiến lược chống dịch hiệu quả cho chính quốc gia đó hay không. Hiện ở Việt Nam có 180 phòng xét nghiệm được Bộ Y tế cho phép thực hiện xét nghiệm khẳng định COVID-19 với công suất khoảng 100.000 xét nghiệm mỗi ngày [21]. Từ năm 2020 đến nay cả nước đã thực hiện xét nghiệm PCR được hơn 2.600.000 mẫu cho 3.500.000 lượt người [22]. Trong thời điểm dịch COVID-19 đang hoành hành như hiện nay, để việc xét nghiệm được hiệu quả, cần tăng cường việc ứng dụng thêm các hình thức test nhanh song song với hình thức PCR truyền thống. Bộ Y tế có thể nhập khẩu thêm các hệ thống test PCR POC để cung cấp cho các khu vực phong tỏa, cách ly, hạn chế việc tới bệnh viện để xét nghiệm, đồng thời tăng số lượng các thiết bị test nhanh kháng nguyên được kiểm định cũng như trợ giá và cải tiến hệ thống phân phối, ứng dụng các kênh bán hàng online để giúp người dân có thể dễ dàng tiếp cận được với xét nghiệm chất lượng nhằm bảo vệ bản thân và cộng đồng.
4. Khuyến cáo cho chiến lược xét nghiệm
Hiện tại, không có phương pháp xét nghiệm nào được xem là lý tưởng; mỗi loại xét nghiệm sẽ đạt được hiệu quả cao nhất nếu được sử dụng đúng chỉ định, cũng như được nhà sản xuất và các cơ quan y tế thông báo đầy đủ đến người sử dụng về đặc điểm và hạn chế. Đối với các trường hợp mới phơi nhiễm, xét nghiệm PCR hữu dụng hơn do chúng có khả năng phát hiện sự tồn tại của virus 2 ngày trước khi bệnh nhân có triệu chứng. Đây cũng được cho là thời điểm mà virus được phóng thích ra môi trường mạnh nhất. Do đó, xét nghiệm phân tử giúp phát hiện ca đang nhiễm, giúp tiến hành kịp thời công tác cách ly và truy vết. Tuy nhiên, cần lưu ý là khi người bệnh đã sắp khỏi bệnh (thông thường là 7 ngày sau khi các triệu chứng bắt đầu xuất hiện) hoặc đã khỏi bệnh thì tải lượng virus thường xuống thấp đến mức không thể được phát hiện bằng xét nghiệm phân tử. Đây sẽ là lúc xét nghiệm kháng thể phát huy hiệu quả, giúp phát hiện được kháng thể trong mẫu máu xét nghiệm và cho thấy được tình trạng miễn dịch của từng bệnh nhân, đặc biệt đối với các trường hợp không triệu chứng, cũng như tình trạng miễn dịch của một cộng đồng nhằm phục vụ các nghiên cứu dịch tễ cũng như các khảo sát tỷ lệ bệnh theo huyết thanh học, nhằm đưa ra cái nhìn đầy đủ nhất về sự lây lan của COVID-19 đồng thời phục vụ công tác truy vết.
Ngoài ra, nhằm hạn chế sai sót trong kết quả, các xét nghiệm PCR cần phải được thực hiện nhiều lần hoặc đi kèm với xét nghiệm kháng thể. Phương pháp này cũng có thể phối hợp với các thiết bị test nhanh hoặc xét nghiệm tại nhà trên diện rộng thông qua việc phân phát đồng thời cả kit xét nghiệm kháng thể và kháng nguyên tại nhà. Test nhanh kháng nguyên nhằm hỗ trợ giám sát dịch bệnh COVID-19, hỗ trợ cho kết quả của RT-PCR, còn test nhanh kháng thể mang tính chất sàng lọc, nghiên cứu, đánh giá dịch tễ. Việc này giúp tăng khung thời gian sàng lọc được ca bệnh đang tiến triển hoặc đã khỏi trong cộng đồng, cho phép cơ quan y tế xử lý kịp thời.
Tài liệu tham khảo
- Health, B., Coronavirus: What is the R number and how is it calculated? 2021.
- Corman, V.M., et al., Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Eurosurveillance, 2020. 25(3): p. 2000045.
- Sheridan, C., Coronavirus and the race to distribute reliable diagnostics. Nature biotechnology, 2020. 38(4): p. 382.
- CDC, Research Use Only Real-Time RT-PCR Protocol for Identification of 2019-nCoV 2020.
- Jacofsky, D., E.M. Jacofsky, and M. Jacofsky, Understanding antibody testing for covid-19. The Journal of Arthroplasty, 2020.
- Li, Z., et al., Development and clinical application of a rapid IgM‐IgG combined antibody test for SARS‐CoV‐2 infection diagnosis. Journal of medical virology, 2020.
- Liu, W., et al., Evaluation of nucleocapsid and spike protein-based enzyme-linked immunosorbent assays for detecting antibodies against SARS-CoV-2. Journal of clinical microbiology, 2020. 58(6).
- Infantino, M., et al., Diagnostic accuracy of an automated chemiluminescent immunoassay for anti‐SARS‐CoV‐2 IgM and IgG antibodies: an Italian experience. Journal of medical virology, 2020.
- VnExpress, 8 loại kit test nhanh nCoV được Bộ Y tế cấp phép. 2021.
- Green, K., et al., What tests could potentially be used for the screening, diagnosis and monitoring of COVID-19 and what are their advantages and disadvantages. The Centre for Evidence Based Medicine (CEBM) https://www. cebm. net/covid-19/what-testscould-potentially-be-used-for-the-screening-diagnosis-and-monitoringof-covid-19-and-what-are-their-advantages-and-disadvantages, 2020.
- Bond, K., et al., Serological tests for COVID-19–a primer. Med. J. Aust, 2020.
- Arevalo-Rodriguez, I., et al., False-negative results of initial RT-PCR assays for COVID-19: a systematic review. medRxiv, 2020.
- Watson, J., P.F. Whiting, and J.E. Brush, Interpreting a covid-19 test result. Bmj, 2020. 369.
- Kucirka, L.M., et al., Variation in false-negative rate of reverse transcriptase polymerase chain reaction–based SARS-CoV-2 tests by time since exposure. Annals of Internal Medicine, 2020.
- Wang, M., et al., Clinical diagnosis of 8274 samples with 2019-novel coronavirus in Wuhan. medRxiv, 2020.
- WHO, Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. 2020.
- Udugama, B., et al., Diagnosing COVID-19: the disease and tools for detection. ACS nano, 2020. 14(4): p. 3822-3835.
- Gorse, G.J., et al., Prevalence of antibodies to four human coronaviruses is lower in nasal secretions than in serum. Clinical and Vaccine Immunology, 2010. 17(12): p. 1875-1880.
- WHO, "Immunity passports" in the context of COVID-19. 2020.
- Xing, Y., et al., Post-discharge surveillance and positive virus detection in two medical staff recovered from coronavirus disease 2019 (COVID-19), China, January to February 2020. Eurosurveillance, 2020. 25(10): p. 2000191.
- tế, B.Y., 180 đơn vị được Bộ Y tế cho phép thực hiện xét nghiệm khẳng định COVID-19. 2021.
- tế, B.Y., Bộ Y tế hướng dẫn sử dụng sinh phẩm xét nghiệm nhanh kháng nguyên vi rút SARS-CoV-2. 2021.